Schubkraft wie beim Tintenfisch: So „schleudern“ schluckbare Kapseln ihren Wirkstoff in den Verdauungstrakt

Den Wasserstrahl-Antrieb von Tintenfischen haben sich Forschende aus den USA und Dänemark zum Vorbild genommen. Das Ergebnis sind oral einnehmbare Kapseln, die ihre flüssige Medikamentenfracht als fokussierten Strahl hervorschießen. Die Geschwindigkeit der Tröpfchen im Strahl soll die Wirkstoffe je nach Behandlungsziel in verschiedene Organe des Verdauungstrakts hinein befördern – ganz ohne Gewebeschäden und Schmerzen zu verursachen.
Die kleinen Geräte sind als angenehmere Alternative zu Injektionen gedacht, mit denen viele Medikamente normalerweise verabreicht werden müssen. Diese können meist nicht oral eingenommen werden, weil sie verdaut würden, bevor sie wirken. Dazu gehören große Proteine wie Insulin und Antikörper etwa, aber auch RNA-basierte Mittel, als Impfstoff oder als therapeutisches Molekül zur Behandlung von Diabetes, Fettleibigkeit und anderen Stoffwechselstörungen.
Entwickler der Kapsel sind Studenten von Giovanni Traverso am Bostoner Massachusetts Institut of Technology (MIT), zusammen mit Wissenschaftlern des ebenfalls in Boston beheimateten Brigham and Women’s Hospital und dem dänischen Pharmaunternehmen Novo Nordisk. Ihre Ergebnisse haben die Forschenden Ende November im Fachjournal Nature veröffentlicht.
Kapselvarianten für den Verdauungstrakt
Tintenfische und andere Kopffüßer wie Kraken bewegen sich durch die Meere, indem sie Wasser in ihre Mantelhöhle saugen und es dann durch eine zweite Öffnung wieder schnell hinauspressen. Dabei steuern die Tiere Richtung und Geschwindigkeit, indem sie die Kraft des Wasserausstoßes dosieren und die Auslassöffnung in verschiedene Richtungen lenken. Aus derselben Öffnung spritzen Kopffüßern bei Gefahr auch gezielt Tintenstrahlen hervor, die ihnen zu einer unbeobachteten Flucht verhilft, während die Sicht der Angreifer vernebelt ist.
Die Forschenden entwickelten mehrere Kapselvarianten für die verschiedene Bereiche des Verdauungstrakts. Die kompaktere, etwa Blaubeer-große Version für geräumigere Organe wie der Magen und der Dickdarm hat ein hoch gewölbtes Dach und einen flachen Boden, in dem die Auslassdüse sitzt und den Wirkstoff axial nach unten, also entlang der Längsachse herausschießt.
Die Dom-Form soll die Kapsel stabilisieren, damit sie sich am Magenboden immer mit der Düse nach unten zur Magenwand hin ausrichtet, selbst dann, wenn der Magen in Bewegung sein sollte. Als Vorbild für die Form dienten große Landschildkröten, die mithilfe der Wölbung wieder auf die Beine zurückrollen, wenn sie mal auf dem Rücken landen. Die Kapsel hat Platz für 80 Mikroliter an Wirkstoff.
Die zweite, längliche Version mit einer Ladekapazität von 200 Mikrolitern ist für den Einsatz in engeren Verdauungsorganen wie die Speiseröhre und der Dünndarm gedacht. Sie ist etwa drei Zentimeter mal ein halber Zentimeter groß und stößt das Medikament seitlich, also radial, durch zwei gegenüberliegende Düsen aus.
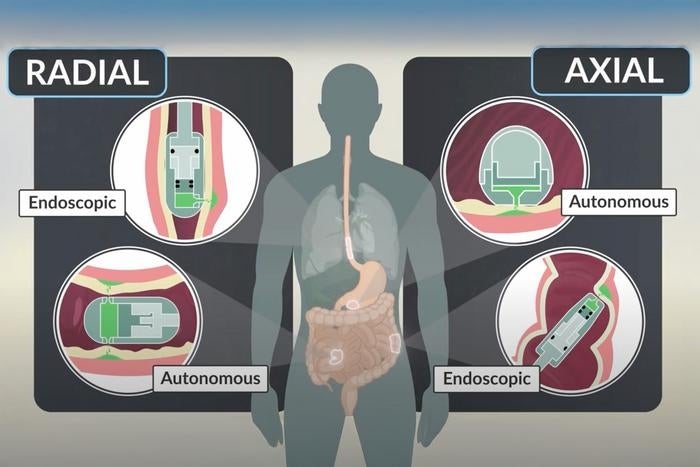
Die Kapselvarianten und wie sie die Wirkstoffe freisetzen. (Grafik: Mit freundlicher Genehmigung der Forscher:innen)
Schleuderkraft durch Gas und Feder
Die beiden Kapseln haben unterschiedliche Auslösemechanismen. In der domförmigen Variante erzeugt komprimiertes Kohlendioxid für die Ausstoßkraft. Die Düsenöffnung ist durch einen Zuckerpropfen verschlossen, den die Magensäure auflöst. Dann dehnt sich das Gas schnell aus und erzeugt die Schubkraft. Für einen verzögerten Einsatz erst im Dickdarm könnten Beschichtungen etwa aus Pektin dafür sorgen, dass der Propfen nur von den Darmenzymen aufgelöst wird, sagt Traverso.
Bei der länglichen Kapsel fixieren ein winziger Rastbolzen und ein äußeres Polymerpellet eine gespannte Feder. Löst sich das auf einen bestimmten pH-Wert eingestellte Pellet auf, dehnt sich die Federn wieder aus und katapultieren die zwei Medikamentenstrahlen hinaus. Die aus Metall und Kunststoff gefertigten Kapseln zerfallen nach der Wirkstofffreigabe und werden wieder ausgeschieden.
„Tröpfchen erzeugen nur vorübergehende Öffnungen im Gewebe“
In Experimenten mit Tiergewebe-Proben aus dem Verdauungstrakt berechneten die Forscher den Druck, der erforderlich ist, um den Wirkstoff mit ausreichender Kraft auszustoßen, damit sie durch die Schleimhaut in das dahinter liegende sogenannte submuköse Gewebe eindringen. Bei den folgenden Tierversuchen haben Biopsien keine feststellbaren Gewebeschäden, Blutungen oder Entzündungen gezeigt, schreiben die Autoren in Nature. „Die Tröpfchen sind kleiner als Injektionsnadeln und erzeugen nur vorübergehende Öffnungen im Gewebe“, erklärt Traverso. „Diese verschließen sich durch die elastischen und regenerativen Eigenschaften der Schleimhautschicht schnell wieder.“
In kleinen Pilotversuchen mit Hunden und Schweinen haben die Forschenden gezeigt, dass sich die Kapseln zum Verabreichen von Insulin, eines GLP-1-Agonisten, das dem Diabetes-Medikament Ozempic ähnelt, und auch von sogenannten short interfering RNA (siRNA) eignen. Mit dieser Art von RNA lassen sich Gene abschalten, was sie potenziell für die Behandlung von genetisch bedingten Krankheiten nützlich macht. Die Wissenschaftler:innen wiesen darüber hinaus nach, dass die Wirkstoffmengen, die aus dem Gewebe ins Blut gelangten, fast oder genau die gleiche war, wie sie Injektionen erreichten.
Neuartige Kapseln statt Injektion per Spritze
Die Forschenden sehen die Kapseln für den heimischen Einsatz für Patienten, die häufig Insulin oder andere injizierte Medikamente brauchen. Sie seien dabei nicht nur für Menschen eine Alternative, die keine Nadeln mögen, sondern könnten auch das Entsorgen der spitzen Nadeln überflüssig machen. Die Forschenden planen, die Kapseln weiter zu verkleinern, damit ihre Passage durch den Körper ähnlich unbemerkt erfolgt wie die von klassischen Medikamentenkapseln. Traverso rechnet damit, dass Versuche mit Menschen in drei bis fünf Jahren starten könnten.
Die Forschung wurde von Novo Nordisk, dem Natural Sciences and Engineering Research Council of Canada, dem MIT Department of Mechanical Engineering, dem Brigham and Women’s Hospital und der U.S. Advanced Research Projects Agency for Health finanziert.
„Die Technologie ist ein bedeutender Fortschritt beim oralen Verabreichen von makromolekularen Arzneimitteln wie Insulin und GLP-1-Agonisten“, sagt Omid Veiseh, ein Bioingenieur von der Rice University, der nicht an der Forschung beteiligt war. Bisherige Ansätze dieser Art seien oft wenig effizient gewesen, transportierten also keine ausreichenden Wirkstoffmengen.

